药品ICH,CTD及eCTD简介--CTD介绍
CTD(The Common Technical Document共同技术文件)是国际公认的文件编写格式,用来制作一个向药品注册机构递交的结构完善的注册申请文件。
一、CTD文件实行的意义:
采用统一的格式将会显著减少企业财力和物力的投入,缩短申请编写的时间,并且将简化电子递交的操作。这些标准化的文件还将有助于注册机构的评审并加强同申请人之间的交流。
此外,在各注册机构之间注册资料的交换也将随之被简化。通过CTD所提供的资料将更加清晰和透明,以利于文件中基础数据的评审和帮助评审人快速定位所申请的内容。
总之,在全球经济一体化的大背景下,采用协调一致的注册申请文件格式也是大势所趋。
CTD共由五个模块组成,模块1是地区特异性的,模块2、3、4和5在各个地区是统一的。具体内容在ICH M4里面体现,其三角结构表如下:
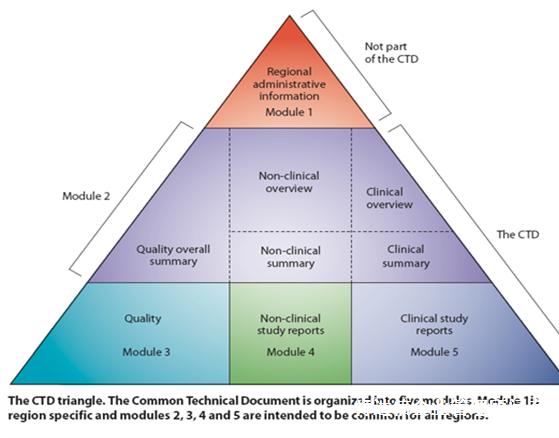
模块1:行政信息和法规信息
本模块包括那些对各地区特殊的文件,例如申请表或在各地区被建议使用的标签,其内容和格式可以由每个地区的相关注册机构来指定。
模块2:CTD文件概述
本模块是对药物质量,非临床和临床实验方面内容的高度总结概括,必须由合格的和有经验的专家来担任文件编写工作。
模块3:质量部分
文件提供药物在化学、制剂和生物学方面的内容。
模块4:非临床研究报告
文件提供原料药和制剂在毒理学和药理学试验方面的内容。
模块5:临床研究报告
文件提供制剂在临床试验方面的内容。
二、CTD文件中关于原料药的部分包括哪些内容?
由于CTD是一个完整的药品上市许可的注册申请文件,所以在CTD文件中,需要我们原料药厂家提交的只是在模块2整体质量概述(The Quality Overall Summary,即QOS)部分和模块3质量(Quality)部分中涉及原料药的化学性质、生产工艺和质量控制等方面的基本数据和资料。在整体质量概述中原料药厂家提供的资料应该能够使质量评审委员对模块3的相关内容有一个大致的了解。
三、 原料药质量部分包括哪些内容?
以模块3质量(Quality)为例,目录如下:
3.2.S原料药(名称,厂商)
3.2.S.1一般信息(名称,厂商)
3.2.S.1.1命名(名称,厂商)
3.2.S.1.2结构(名称,厂商)
3.2.S.1.3一般性质(名称,厂商)
3.2.S.2生产(名称,厂商)
3.2.S.2.1厂商(名称、厂商)
3.2.S.2.2生产工艺和工艺控制的描述(名称、厂商)
3.2.S.2.3物料控制(名称、厂商)
3.2.S.2.4关键步骤和关键中间体的控制(名称、厂商)
3.2.S.2.5工艺验证和/或评估(名称、厂商)
3.2.S.2.6生产工艺研究(名称,厂商)
3.2.S.3特征(名称,厂商)
3.2.S.3.1结构和其它特征的确认(名称、厂商)
3.2.S.3.2杂质(名称,厂商)
3.2.S.4原料药的控制(名称、厂商)
3.2.S.4.1质量标准(名称、厂商)
3.2.S.4.2分析规程(名称、厂商)
3.2.S.4.3分析规程的验证(名称、厂商)
3.2.S.4.4批分析(名称、厂商)
3.2.S.4.5质量标准说明(名称、厂商)
3.2.S.5参照标准品或物质(名称、厂商)
3.2.S.6容器密封系统(名称、厂商)
3.2.S.7稳定性(名称、厂商)
3.2.S.7.1稳定性总结和结论(名称、厂商)
3.2.S.7.2批准后的稳定性方案和稳定性建议(名称、厂商)
3.2.S.7.3稳定性数据(名称、厂商)
四、肯达信企业管理顾问有限公司的服务流程:
发出《客户资料表》→评估(电话、邮件、现场)→出具合同和计划表→签订合同→现场诊断→分析原因→出具详细计划表→专业知识培训→指导准备申报所需中文资料→翻译制作相关格式英文文件→递交文件给官方→保持联络→指导完成缺陷补充资料→批准→证后变更及维护。