进口保健食品注册代理---进口(含港、澳、台)保健食品产品注册
提供的样品包装应完整、无损,应贴有标签,标签应与申报资料中相应的内容一致。样品包装应利于样品的保存,不易变质、破碎。样品应在保质期内。
23、上述申报资料必须使用中文并附原文,外文的资料可附后作为参考。中文译文应当由境内公证机关进行公证,确保与原文内容一致;申请注册的产品质量标准(中文本),必须符合中国保健食品质量标准的格式。
24、还应当注意以下事项:
(1)产品注册申请表中,进口产品申请人为产品所有权的拥有者,生产企业为产品的实际生产者(申报产品由申请人自行生产的,生产企业即为申请人;申报产品由申请人委托境外其他企业生产的,生产企业即为被委托企业)。
(2)产品名称、申请人名称、生产企业名称、代理机构名称(中、英文)应前后一致。
(3)证明文件、委托书应为原件,应使用生产国(或地区)的官方文字,需由所在国(或地区)公证机关公证和我国驻所在国使(领)馆确认。
(4)证明文件、委托书中载明有效期的,应当在有效期内使用。
(5)证明文件、委托书应有单位印章或法人代表(或其授权人)签字。
八、申办流程示意图:
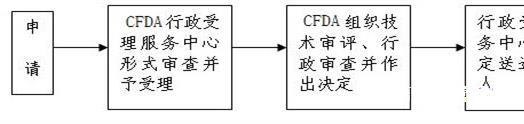
九、许可程序:
(一)受理:
申请人向行政受理服务中心提出申请,按照本《须知》第六条所列目录提交申请材料,受理中心工作人员按照“《保健食品注册管理办法》附件一:进口保健食品产品注册申请申报资料项目”对申请材料进行形式审查。申请事项依法不需要取得行政许可的,应当即时告知申请人不受理;申请事项依法不属于本行政机关职权范围的,应当即时作出不予受理的决定,并告知申请人向有关行政机关申请;申请材料存在可以当场更正的错误的,应当允许申请人当场更正;申请材料不齐全或者不符合法定形式的,应当当场或者在五日内一次告知申请人需要补正的全部内容,逾期不告知的,自收到申请材料之日起即为受理;申请事项属于本行政机关职权范围,申请材料齐全、符合法定形式,或者申请人按照本行政机关的要求提交全部补正申请材料的,应当受理行政许可申请。
(二)检验与核查:
行政受理服务中心受理后,国家食品药品监督管理总局在5日内向确定的检验机构发出检验通知书并提供检验用样品。根据需要,国家局可以对该产品的生产现场和试验现场进行核查。
检验机构收到检验通知书和样品在50日内对抽取的样品进行样品检验和复核检验,将检验报告移送国家食品药品监督管理总局,同时抄送申请人。特殊情况,检验机构不能在规定的时限内完成检验工作的,应当及时向国家食品药品监督管理总局报告并书面说明理由。
(三)技术审评和行政审查:
国家食品药品监督管理总局在受理申请后,应当在80日内对申报资料进行技术审评和行政审查,并作出许可决定。在审查过程中,需要补充资料的,国家食品药品监督管理总局应当一次性提出。申请人应当在收到补充资料通知书后的5个月内提交符合要求的补充资料,未按规定时限提交补充资料的予以退审。特殊情况,不能在规定时限内提交补充资料的,必须向国家食品药品监督管理总局提出书面申请,并说明理由。国家食品药品监督管理总局应当在20日内提出处理意见。申请人补充资料时间不计入许可时限,其审查时限在原审查时限的基础上延长30日。经审查准予注册的,发给《国产保健食品批准证书》。不予注册的,应当书面说明理由。
(四)送达:
自行政许可决定作出之日起10日内,CFDA行政受理服务中心将行政许可决定送达申请人。
(五)复审:
申请人对国家食品药品监督管理总局作出的不予注册的决定有异议的,可以在收到不予注册通知之日起10日内向国家食品药品监督管理总局提出书面复审申请并说明复审理由。
国家食品药品监督管理总局收到复审申请后,应当按照原申请事项的审查时限和要求进行复审,并作出复审决定。撤销不予注册决定的,向申请人颁发相应的保健食品批准证明文件;维持原决定的,不再受理再次的复审申请,但申请人可按照有关法律规定,向国家食品药品监督管理总局申请行政复议或者向人民法院提起行政诉讼。
十、承诺时限:
自受理之日起,85日内作出行政许可决定。
十一、实施机关:
实施机关:国家食品药品监督管理总局
受理地点:国家食品药品监督管理总局行政受理服务中心
十二、许可证件有效期与延续:
《进口保健食品批准证书》有效期为5年,《进口保健食品批准证书》有效期届满需要延长有效期的,申请人应当在有效期届满三个月前申请再注册。
十三、许可年审或年检:无
十四、受理咨询与投诉机构:
咨询:国家食品药品监督管理总局
投诉:国家食品药品监督管理总局驻局监察局、法制司
注:本须知工作期限以工作日计算,不含法定节假日